
Die Rolle von CRISPR im Mikrobiom-Engineering [Podcast]
Die Rolle von CRISPR bei wissenschaftlichen Durchbrüchen im Mikrobiom-Engineering
Clustered Regularly Interspaced Short Palindromic Repeats (CRISPR) wurden erstmals im Genom von Meeresbakterien entdeckt. Bei einer Virusbedrohung entwickelten Bakterienzellen eine Immunantwort, indem sie DNA-Fragmente von Viren einfangen und kopieren. Dies ermöglichte es Bakterien, nachfolgende Attacken zu erkennen und die virale DNA zu spalten, um die Virusinfektion zu stoppen. Es wurde auch herausgefunden, dass das Cas-Enzym für die DNA-Spaltung verantwortlich war. Dieser Abwehrmechanismus wurde später von Doudna und Charpentier genutzt, die eine bestimmte DNA-Sequenz gezielt isolieren und mit dem CRISPR-Cas9-System (1) isolieren konnten.
In den letzten zehn Jahren hat sich CRISPR-Cas9 in der Wirkstoffforschung und Wirkstoffherstellung als äußerst wertvoll erwiesen. Mithilfe einer synthetischen Leit-RNA (gRNA) können Wissenschaftler eine bestimmte DNA-Sequenz anvisieren und Cas9 zum Schneiden verwenden. Anschließend versucht die Wirtsreparaturmaschinerie, die DNA durch nicht-homologe Endverbindung (NHEJ) zu reparieren, was zu zufälligen Mutationen führt, die die Genfunktion verändern. Mithilfe dieses Mechanismus konnten Wissenschaftler nun Gene stummschalten, um ihre Rolle im Krankheitsphänotyp aufzuklären, was der Target-Discovery zugutekommen kann. Darüber hinaus können Wissenschaftler CRISPR-Cas9 auch verwenden, um Mechanismen der Arzneimittelresistenz aufzudecken, indem sie die Genreihe identifizieren, die mit der Umgehung des Immunsystems assoziiert ist.
Heute werden wir jedoch eine andere Anwendung von CRISPR untersuchen: Mikrobiom-Engineering. Die kürzlich von Molecular Devices ins Leben gerufene Folge des Podcasts über die Überprüfung von Wirkstoffzielen erörtert die Anwendung von CRISPR im Mikrobiom-Engineering und wie es den Engpass der menschlichen Mikrobiomforschung überwinden kann.
Schließen Sie sich den führenden Experten Dr. Jakob Haaber , Vice President & Head of Delivery Technologies, SNIPR Biome und Dr. Richard Fox , Co-Founder, CEO und CTO von Infinome Biosciences, an, um die breite Palette an Anwendungen für CRISPR zu diskutieren, einschließlich für Therapeutika und Biomanufacturing.
Wie CRISPR-Cas9 die Erforschung der Rolle des menschlichen Mikrobioms bei Krankheiten unterstützt
Inzwischen ist bekannt, dass der menschliche Körper Billionen von Mikroorganismen enthält und somit menschliche Zellen übertrifft. Diese Mikroorganismen werden zusammen als Mikrobiom bezeichnet und bilden eine Symbiose mit dem Körper, indem sie die extrazelluläre Umgebung regulieren und die Zellen vor Pathogenen schützen. Daher ist es nicht überraschend, dass Störungen im Mikrobiom eng mit zahlreichen Krankheiten verbunden sind, von Diabetes und Fettleibigkeit bis hin zu Krebs.
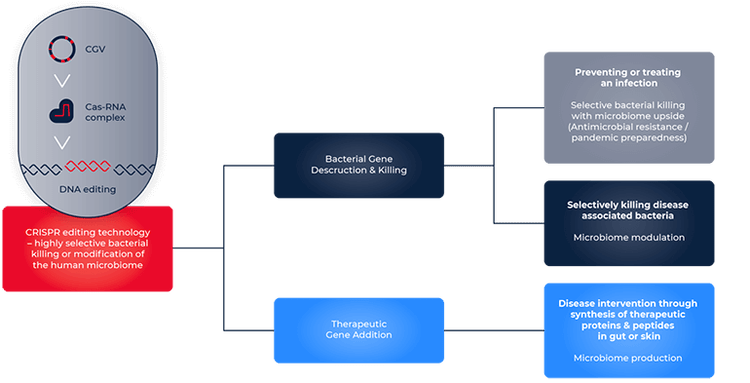
Eine Möglichkeit, wie CRISPR zur Wirkstoffforschung beiträgt, ist seine Implementierung zur Abmilderung der Störungen im Mikrobiom. Dies wird durch die Entwicklung von CRISPR-Cas9-Systemen erreicht, um spezifische bakterielle DNA-Sequenzen zu schneiden und pathogene Bakterien zu eliminieren. SNIPR Biome ist eines der Unternehmen, die aktiv an diesem Ziel arbeiten. Dr. Jakob Haaber, Vice President und Head of CRISPR and Delivery Technologies bei SNIPR Biome, beschreibt die Anwendung von CRISPR auf die pathogene E. coli-Elimination: „Wir zielen auf sie ab, indem wir unseren CRISPR anwenden, den wir programmiert haben, um E. coli zu töten. Gegenwärtig ist die Behandlung von bakteriellen Infektionen mit Antibiotika unumgänglich. Es kommt jedoch häufiger zu einer Antibiotikaresistenz, wodurch Antibiotika unwirksam werden. Der Vorteil von CRISPR besteht darin, dass es nicht zwischen antibiotikaempfindlichen und antibiotikaresistenten Bakterien unterscheidet. Er schlägt auch vor, dass CRISPR gezielt gegen pathogene Bakterien gerichtet sein und die nützlichen Bakterien, die für das gesunde Darmmikrobiom von wesentlicher Bedeutung sind, erspart, im Gegensatz zu Antibiotika mit nachteiligen Auswirkungen auf gesunde Bakterien neben Pathogenen.
Vorteile von CRISPR und jüngste Entwicklungen
Laut Richard Fox, Mitbegründer, CEO und CTO von Infinome Biosciences, liegt die Hauptstärke von CRISPR in seiner Fähigkeit, das Genom-Editing zu erweitern. „Anstelle von zufälligen Mutationen auf einem kleinen Satz von Zielgenen können wir jetzt einen gesamten Signalweg oder ein ganzes Genom präzise bearbeiten und Hunderttausende von Veränderungen einführen.“
Das Genom-Editing im großen Maßstab ermöglicht kommerziell erhältliche Zellbibliotheken, die Forscher in ein phänotypisches Screening mit hohem Durchsatz integrieren können. Diese Bibliotheken machen es überflüssig, eine große Anzahl von Genen für das phänotypische Profiling manuell auszuknocken und bieten eine Lösung für die Beschleunigung von Wirkstoffforschungsstudien.
Ein weiterer Vorteil der CRISPR-Technologien ist die verbesserte Spezifität. Mikrobiomgen-Editing ist eines der Felder, die die Vorteile der Spezifität nutzen. CRISPR-Systeme können so programmiert werden, dass sie spezifische bakterielle DNA schneiden oder sogar genetische Schaltkreise innerhalb der Zellwände von Bakterien entfernen, ohne die Zelle abzutöten. Zusammengenommen fördern diese Fortschritte neuartige Gentherapien für Abweichungen von Darmmikrobiota.
In der Zwischenzeit haben CRISPR-Systeme die Herstellung kleinerer genetischer Konstrukte ermöglicht, um das Packen in Lieferfahrzeuge zu erleichtern. Somit kann der Trägerstoff neben CRISPR mehrere Komponenten tragen, was ein multifunktionales Gen-basiertes Therapeutikum darstellt, das viel mehr als nur das Schneiden oder Einfügen von DNA ermöglicht.
Beschleunigung bei der Herstellung von CRISPR-Technologien
Die Lücke zwischen synthetischer Biologie und Bioengineering wird häufig durch Zeit- und Kostenprobleme verursacht. Um eine Biomanufacturing-Lösung auf den Markt zu bringen, sind große Unternehmen mit gut aufgebauter Infrastruktur, robuster Automatisierung, vielen Menschen, Instrumenten, Informatik und viel Kapital erforderlich. Daher ist es nicht überraschend, dass die Entwicklung von Biologika 5Jahre10 und viele Millionen Dollar in Anspruch nehmen kann. Dies ist eine recht riskante Investition, daher zögern Pharmaunternehmen oft, sich daran zu beteiligen, was Gebiete mit einem enormen therapeutischen Potenzial unerforscht lässt.
Die Einrichtung des CRISPR-fähigen Genom-Editing-Systems ist einer der Engpässe in Arbeitsabläufen. Das Design von Genome-Engineering-Systemen im großen Maßstab ist ziemlich mühsam, da man möglicherweise winzige Mengen an Spendersequenzen produzieren muss, um 10.000 Loci gezielt zu bearbeiten und präzise in ein ganzes Genom zu bearbeiten.
Andrew Garst, einer der Mitbegründer von Infinome Biosciences, entwickelte eine Schlüsselinnovation, indem er die Führungssequenz koppelte, die den Schnitt mit der Spendersequenz lenkt, die die Reparatur vermittelt, und so die Bearbeitung breiter Genome auf wenige Klicks reduzierte. Richard Fox ist der Ansicht, dass „solche automatisierten Design- und Build-Systeme in weniger als einer Woche bearbeitete Zellbibliotheken erstellen können, was dem Bruchteil des Aufwands entspricht, den sie früher aufgewendet haben“.
Schritte des mikrobiellen Gen-Editings
Der erste Schritt im Gen-Editing für das Darmmikrobiom ist die In-vitro-Validierung des CRISPR-Systems. Die Spezifität der CRISPR-Editierung wird mit einer Reihe von Bakterienpanels getestet, die für das Darmmikrobiom repräsentativ sind. Ziel ist es, sicherzustellen, dass das CRISPR-System auf eine vorher festgelegte Unterart von Bakterien abzielt und dass die nützlichen Bakterien von der CRISPR-induzierten Gen-Editierung ausgenommen sind.
Dann geht die Validierung zu den präklinischen und klinischen Studien über. Mithilfe von Genomsequenzierungstechniken demonstrieren Forscher, dass das Gen-Editing das Mikrobiom nicht auf schädliche Weise beeinträchtigt. Natürlich können Off-Target-Effekte unvermeidlich auftreten, wie die Gesamtgenomsequenzierung zeigt. Die Vorgehensweise besteht darin, die Häufigkeit des Auftretens zu überwachen und sicherzustellen, dass diese Effekte trivial sind und das Gen-Editing nicht beeinträchtigen.
Die Sequenzierung und das phänotypische Profiling zeigen die Bearbeitungen, die ein Genom mit sich bringt, sowie die vorherrschenden Stämme in einer Bakterienpopulation. Um den Erfolg der gezielten Genom-Editierung weiter zu validieren, kann man die Bakterienpopulation Umweltstressoren aussetzen und deren Verhalten überwachen. Dadurch wird sichergestellt, dass das Gen-Editing den Bakterien die gewünschten Eigenschaften verleiht, z. B. die Fähigkeit, unter Umweltbelastung wie Hypoxie zu wachsen.

Mit beschleunigten CRISPR-Arbeitsabläufen können Forscher eine Reihe vorteilhafter Gen-Edits unter Hunderttausenden von Gen-Knockouts erzielen.
CRISPR-Systeme bieten zudem die Flexibilität, denselben Bakterienstamm je nach spezifischem Forschungsbedarf anzureichern oder zu depletieren. Forscher bei Infinome haben zum Beispiel CRISPR implementiert, um E. coli-Stämme zu entwickeln und die Lysinproduktion, eine wichtige Aminosäure, die als Lebensmittelzusatzstoff verwendet wird, zu vergrößern. Auf der anderen Seite verwendete SNIPR dasselbe System, um schädliche E. coli-Stämme aus dem Darm von Patienten mit hämatologischem Krebs zu entfernen und so Infektionen des Blutkreislaufs zu verhindern.
Blick in die Zukunft von CRISPR
Wie bereits erwähnt, befähigt CRISPR den Kampf gegen pathogene Bakterien. Es hat sich mehrfach bewährt, dass konventionelle Antibiotikabehandlungen die Darmmikrobiota durch das Abzielen auf schädliche und nützliche Bakterien stören. CRISPR kann dazu beitragen, die Spezifität von Bakterien zu verbessern, um das Gleichgewicht der menschlichen Darmmikrobiota aufrechtzuerhalten.
Ein weiterer spannender Aspekt von CRISPR ist die Fähigkeit, Bakterienstämme mit therapeutischem Potenzial zu entwickeln. Dies kann verwendet werden, um dem Mikrobiom durch technisch veränderte Bakterien genetische Funktionen hinzuzufügen, die ein spezifisches Enzym oder einen spezifischen Metaboliten exprimieren können, das/den der Körper zuvor nicht kannte.
Die erfolgreiche Umsetzung von CRISPR im biomedizinischen und bioindustriellen Ingenieurswesen beruht schließlich auf der Fähigkeit, kombinatorische Änderungen vorzunehmen, die auch als „DNA-Shuffling“ bezeichnet werden. Vor allem bei großen mikrobiellen Systemen ist die Möglichkeit, mehrere Bearbeitungen zur Reduzierung der Anzahl der Screening-Runden einzuführen, von höchster Bedeutung für die Umsetzung der bioindustriellen Produktion.
Molecular Devices unterstützt Wissenschaftler durch die Bereitstellung modernster Technologien, die das unmittelbare Ziel des CRISPR-Cas9 Genom-Editings beschleunigen. Ein genaues Bibliotheksscreening und die Auswahl der CRISPR-editierten Treffer ist der Schlüssel zu Arbeitsabläufen im Mikrobiom-Engineering und ermöglicht eine schnellere Verfügbarkeit des Biomanufacturing-Produkts auf dem Markt.
- Doudna, Jennifer A. und Emmanuelle Charpentier. „Die neue Grenze des Genome Engineering mit CRISPR-Cas9.“ Wissenschaft 346,6213 ( 2014): 1258096.
CRISPR在微生物组工程科学突破中的作用
CRISPR首次在海洋细菌的基因组中发现,当面临病毒威胁时,细菌细胞通过捕获和复制病毒的DNA片段来产生免疫反应,这使得细菌能够识别随后的攻击并切割病毒DNA以阻止病毒感染。另外,还发现Cas酶负责切割DNA,这种防御机制后来被Doudna和Charpentier利用,他们可以靶向目标DNA序列,并使用CRISPR-Cas9系统将其分离(1)。
在过去的十年中,CRISPR-Cas9已被证明在药物发现和药物制造中具有巨大的价值。使用合成向导RNA(gRNA),科学家可以靶向目标DNA序列并使用Cas9进行切割。随后,宿主修复机制试图通过非同源末端连接(NHEJ)修复DNA,导致改变基因功能的随机突变。利用这种机制,科学家们现在可以使基因沉默来阐明它们在疾病表型中的作用,这有利于发现目标。此外,科学家还可以利用CRISPR-Cas9,通过识别与免疫系统逃避相关的一组基因来揭示耐药机制。
然而,今天,我们将探索CRISPR的不同应用:微生物组工程。本期内容我们来讨论CRISPR在微生物组工程中的应用以及它如何克服人类微生物组研究的瓶颈。
本次嘉宾:Jakob Haaber博士,副总裁兼交付技术主管SNIPR Biome和Infinome Biosciences联合创始人、CEO 兼CTO Richard Fox博士一起探讨CRISPR的广泛用途,包括治疗和生物制造。
CRISPR-Cas9如何帮助探索人类微生物组在疾病中的作用
众所周知,人体含有数万亿种微生物,在数量上超过了人体细胞。这些微生物统称为微生物组,通过调节细胞外环境和保护细胞免受病原体侵害,与人体形成共生关系。因此,从糖尿病、肥胖到癌症,微生物组的破坏与许多疾病密切相关也就不足为奇了。

通过设计CRISPR-Cas9系统来切割特定的细菌DNA序列以消除致病细菌,这种特异性使CRISPR技术减轻对整体微生物组的破坏,实现药物发现进程的加速。。SNIPR Biome是积极致力于实现这一目标的公司之一,SNIPR Biome副总裁兼CRISPR负责人和交付技术主管Jakob Haaber博士描述了CRISPR在致病性大肠杆菌消除中的应用:“我们使用CRISPR杀死大肠杆菌。目前,治疗细菌感染最常用的就是抗生素。但抗生素耐药性的发生率增加,进而使抗生素无效。CRISPR的优点是它不区分抗生素敏感和抗生素耐药细菌。他还建议,CRISPR可以专门针对致病细菌,而不影响健康肠道微生物组中不可或缺的有益细菌,而不是像抗生素一样,对健康细菌和病原体都有影响。
CRISPR的优势和近年发展

Infinome Biosciences的联合创始人、CEO兼CTO Richard Fox表示,CRISPR的主要优势在于其扩大基因组编辑的能力。“我们现在可以精确地编辑整个通路或基因组,而不是一小部分目标基因上的随机突变,从而引入数十万个变化。
大规模的基因组编辑产生可商用的细胞库,研究人员可以将其整合到高通量表型筛选中。这些库消除了手动敲除大量基因进行表型分析的需要,并为加速药物发现研究提出了解决方案。
CRISPR技术的另一个优点是提高了特异性,微生物组基因编辑是受益于特异性的领域之一。CRISPR系统可以被编程为切割特定的细菌DNA,甚至在不杀死细胞的情况下去除细菌细胞壁内的基因回路。综上所述,这些进步推动了肠道微生物群偏差的新基因疗法。
与此同时,CRISPR系统已经能够制造出更小的基因构建体,以便更容易地装配到递送载体中。因此,除了CRISPR之外,递送载体还可以携带多种成分,构成一种多功能的基于基因的疗法,不仅仅是切割或插入DNA。
加速CRISPR技术的制造
合成生物学和生物工程之间的差距通常是由时间和成本问题引起的。将生物制造解决方案推向市场需要大型实体,这些实体具有完善的基础设施、强大的自动化、大量的人员、仪器、信息学和大量资金。因此,生物制剂的开发可能需要5-10年和数百万美元也就不足为奇了。这是一项风险相当大的投资,因此制药公司往往不愿参与其中,从而一些具有巨大治疗潜力的领域未得到开发。
支持CRISPR的基因组编辑系统的设置是工作流程的瓶颈之一。大规模基因组工程系统的设计非常费力,因为需要产生微量的供体序列来靶向并精确地将10,000个位点编辑到整个基因组。
Infinome Biosciences的联合创始人之一Andrew Garst提出了一项关键创新,将指导切割的引导序列与介导修复的供体序列配对,从而将广基因组编辑减少到只需点击几下。Richard Fox认为,“这种自动化设计和构建系统可以在不到一周的时间内创建编辑过的细胞库,这是过去所花费的努力的一小部分”。
微生物基因编辑步骤
肠道微生物组基因编辑的第一步是CRISPR系统的体外验证。CRISPR编辑的特异性是针对一组代表肠道微生物组的细菌进行测试的,以确保CRISPR系统针对预定的细菌亚种,并且使得有益细菌不受CRISPR诱导的基因编辑的影响。
然后,验证继续进行到临床前和临床研究。利用基因组测序技术,研究人员证明基因编辑不会以有害的方式扰乱微生物组。当然,脱靶效应不可避免地会发生,正如全基因组测序所揭示的那样。我们需要做是监测发生率,并确保这些影响是微不足道的,不会干扰基因编辑。
测序和表型分析揭示了基因组携带的一组编辑以及细菌种群中的主要菌株。为了进一步验证靶向基因组编辑的成功,可以将细菌种群置于环境压力源中并监测其行为。这确保了基因编辑赋予细菌所需的特性,例如在缺氧等环境压力下生长的能力。

通过加速的CRISPR工作流程,研究人员可以在数十万个基因敲除中得到一组有益的基因编辑。
CRISPR系统还可以根据特定的研究需求,灵活地富集或消耗相同的细菌菌株。例如,Infinome的研究人员应用CRISPR来设计大肠杆菌菌株,以扩大赖氨酸的生产,赖氨酸是一种用作食品添加剂的关键氨基酸。另一方面,SNIPR使用相同的系统从血液癌患者的肠道中根除有害的大肠杆菌菌株,以防止血液感染。
展望
如前所述,CRISPR能够对抗致病菌,已多次证明,传统的抗生素治疗通过作用有害和有益细菌来破坏肠道微生物群。CRISPR可以帮助增强细菌的特异性,以维持人类肠道微生物群的平衡。
另一个令人兴奋的前景是设计具有治疗潜力的细菌菌株的能力。这可用于通过工程细菌为微生物组添加遗传功能,这些细菌可以表达身体以前缺乏的特定酶或代谢物。
最后,CRISPR在生物医学和生物工业工程中的成功应用依赖于进行组合编辑的能力,也称为“DNA洗牌”。特别是在大型微生物系统中,引入多次编辑以减少筛选轮次的能力对于生物工业生产至关重要。
Molecular Devices通过提供前沿技术来帮助科学家加速CRISPR-Cas9基因组编辑的近期目标。准确的文库筛选和CRISPR编辑命中物的选择是微生物组工程工作流程的关键,使生物制造产品更快地推向市场。
1. Doudna, Jennifer A.和Emmanuelle Charpentier。“CRISPR-Cas9基因组工程的新前沿。科学346,6213(2014):1258096。