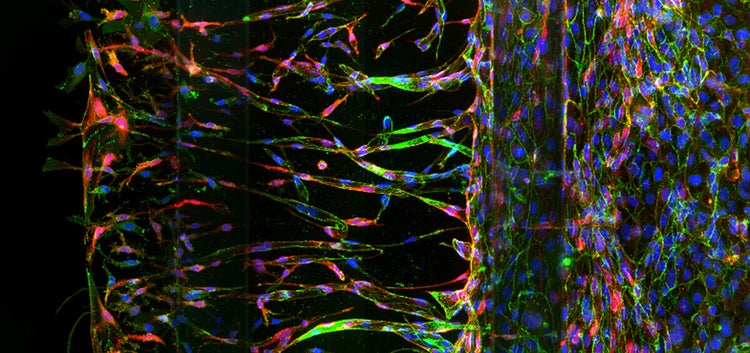
3D-High-Content-Imaging und -Analyse auf einer Organ-on-a-Chip-Plattform ermöglichen
Stellen Sie sich vor, Sie könnten die biologische Umgebung eines menschlichen Körpers für die Modellierung von Krankheiten und das Screening von Wirkstoffen nachahmen – und dies in einem Mikromaßstab-System. Mit der Entwicklung von Organ-on-a-Chip-Modellen ist dies nicht mehr unplausibel. Durch die Integration von Mikrofluidik mit Zellen und Wachstumsfaktoren können Wissenschaftler nun biologisch relevante Modelle erzeugen, die das physiologische und mechanische Verhalten des tatsächlichen Gewebes nachahmen.
Durch die erfolgreiche Implementierung können Organ-on-a-Chip-Modelle erhebliche Zeit in der Wirkstoffforschung sparen und eine schnellere und genauere Beurteilung der Pharmakokinetik, Wirksamkeit und Zytotoxizität sowie die personalisierte medizinische Forschung ermöglichen.
In einer nicht so weit entfernten Zukunft werden wir weniger von Tiermodellen für Tests zur Wirkstoffentwicklung und Toxizitätsbewertung abhängig sein, da sie In-vivo-Bedingungen genauer nachahmen.
Diese mikroskaligen Organsysteme wurden entwickelt, um die Feinheiten der menschlichen Biologie besser darzustellen. Ihre Komplexität stellt jedoch Herausforderungen im Bereich des Imaging im großen Maßstab dar, um quantitative und reproduzierbare Ergebnisse zu erzielen.
Die bahnbrechende Zusammenarbeit zwischen Molecular Devices und MIMETAS, einem weltweit führenden Anbieter von Organ-on-a-Chip-Modellen, kann uns dabei helfen, zu demonstrieren, wie wir diese Herausforderungen des 3D-High-Content-Imaging meistern können.
Was ist ein Organ-on-a-Chip?
Organs-on-Chips sind Mikrofluidik-basierte Zellkulturgeräte, die die Größe eines Memory-Sticks haben und die komplexen Strukturen und Prozesse menschlicher Organe nachbilden können. Sie bestehen aus einem flexiblen und transparenten Biopolymer mit winzigen Hohlkanälen, die lebende menschliche Zellen enthalten.
Durch die gezielte Anordnung und Abtrennung verschiedener Zelltypen kann man die Interaktionen zwischen anderen Gewebezellen im Organ simulieren und kontrollieren. Eine poröse Membran trennt üblicherweise die Mikrokanäle, um interzelluläres Crosstalk zu ermöglichen, wie z. B. die Interaktionen zwischen Endothel- und Epithelzellen.
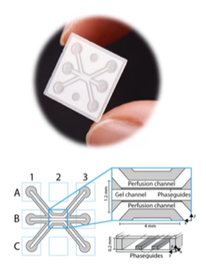
OrganoPlate: Die hochmoderne Lösung von MIMETAS für die Gewebemodellierung
2014MIMETAS wurde in Leiden, Niederlande, gegründet und ist ein Pionier der Organ-on-a-Chip-Modelle, die die Erforschung menschlicher Krankheitsmodelle ermöglichen. Ihre wichtigste Innovation, OrganoPlate®, ist eine auf Mikrofluidik basierende Plattform, die bis zu 96 Gewebemodelle auf einer einzigen Platte unterstützt.
OrganoPlate verdankt seine Vielseitigkeit und Einfachheit der PhaseGuide™ Technologie. Im Gegensatz zu herkömmlichen Organ-on-Chips ermöglicht die patentierte Liquid-Handling-Technologie die membranfreie Bildung extrazellulärer Matrizen in 3D . Dies ermöglicht die freie Bewegung und Interaktion von Zellen und die Einführung von Proteinen und Co-Kulturverbindungen.

Die Mikrofluidik-Netzwerke in OrganoPlate ermöglichen einen kontinuierlichen mittleren Fluss ohne externe Pumpen oder Schläuche. Die Bewegung von Nährstoffen, Sauerstoff, Wachstumsfaktoren und Kokulturbedingungen wird durch eine durch Schwerkraft gesteuerte Technologie vermittelt. Dies führt zu einer kontinuierlichen Perfusion, die den Blutfluss nachahmt. Diese Faktoren machen OrganoPlate zu einer ausgezeichneten Quelle für die Untersuchung der Durchlässigkeit, Migration, des Auswuchses, der Invasion, Angiogenese und komplexer Zell-Zell-Interaktionen.
3D-High-Content-Imaging-Lösungen für Organ-on-a-Chip
Da Organ-on-a-Chip-Modelle mit verschiedenen Assays kompatibel sind, von der Immunfärbung über die Überlebensfähigkeit bis hin zur qPCR, sind die Überwachung und Analyse der Ergebnisse oft komplexer als 2D-In-vitro-Modelle.
Die gute Nachricht ist, dass OrganoPlate einen Glasboden in Mikroskopiequalität enthält, der es zum einzigen Organ-on-a-Chip-Modell macht, das sich für das High-Throughput- und High-Content-Imaging eignet.

MIMETAS hat mit Molecular Devices zusammengearbeitet, um seine Fähigkeiten und Geräte im 3D-High-Content-Imaging zu verbessern. Eines der jüngsten Produkte dieser Zusammenarbeit ist die Installation des neuen ImageXpress® Micro Confocal High-Content Imaging System von Molecular Devices . Um noch einen Schritt weiter zu gehen, bieten wir den Kunden von MIMETAS personalisierte Schulungen an. Forscher können lernen, Organ-on-a-Chip-Experimente auf OrganoPlate zu entwerfen und durchzuführen und die 3D-Zellkulturen mit dem ImageXpress Micro Confocal abzubilden.
Sehen wir uns nun an, wie dies auf bestimmte Gewebemodelle zutrifft.
Angiogenese
Die Angiogenese umfasst die Bildung neuer Blutgefäße sowie die Regeneration beschädigter Blutgefäße. Es ist nicht nur ein integraler Bestandteil des Gewebewachstums, der Gewebeentwicklung und -reparatur, sondern ein häufiges Phänomen bei der Tumorinvasion und -metastasierung. Daher kann ein erfolgreiches Imaging angiogener Mechanismen Türen zur Entdeckung antiangiogener Krebsmedikamente öffnen. Derzeitige In-vitro-Assays bieten jedoch nur begrenzte Einblicke und veranschaulichen nicht die endotheliale Sprossung und das Gefäßwachstum.
Die OrganoPlate-Plattform bietet Forschern ein fundierteres Modell zur Quantifizierung und Visualisierung der Anzahl und Größe angiogener Sprosse sowie angiogener Marker für die Proliferation und Expression.
Während der ersten Angiogenese-Studie, die von MIMETAS mit Molecular Devices durchgeführt wurde, wurde OrganoPlate 3-spurig verwendet, um das Angiogenese-Modell zu entwickeln. Jeder der 40Chips in OrganoPlate bestand aus drei Kanälen mit folgendem Inhalt von oben nach unten: Endothelzellen, Kollagen-I-Gel der extrazellulären Matrix (ECM) und angiogene Faktoren. Wie in der Application Note, 3D Image Analysis and Characterization of Angiogenesis in Organ-on-a-Chip Model dargestellt, wurde die Bildung von angiogenen Sprossen in den nächsten vier Tagen überwacht.
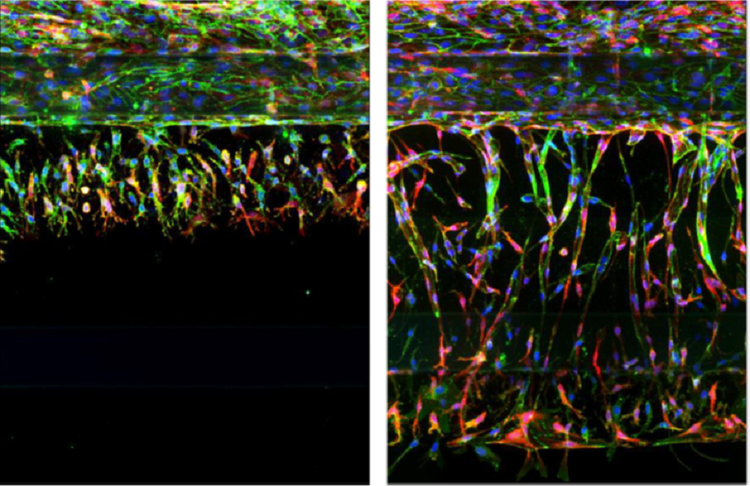
Tag 1 (links) und Tag 4 (rechts) der angiogenen Sprossen in OrganoPlate mit 20X Vergrößerung.
Die Zellkerne, das Zelladhäsionsmolekül VE-Cadherin und die Aktinfilamente von Endothelzellen wurden unterschiedlich gefärbt. Mit dem konfokalen Modus des ImageXpress Micro Confocal High-Content Imaging System konnten Forscher Sprossen nach 1 Tag und 4 Tagen in der Kultur visualisieren. Weitere Analysen dieser Bilder wurden mit dem Custom Module Editor (CME) in der MetaXpress® High-Content Image Acquisition and Analysis Software durchgeführt. Diese Analyse lieferte wertvolle Einblicke in das zeitabhängige Wachstum der Gefäße, indem sie verschiedene Faktoren wie die Gesamtzahl der Sprossen, die Anzahl der Zellkerne pro Sprossen, das Volumen, die Intensität und die Abstände zwischen den Sprossen aufdeckte.
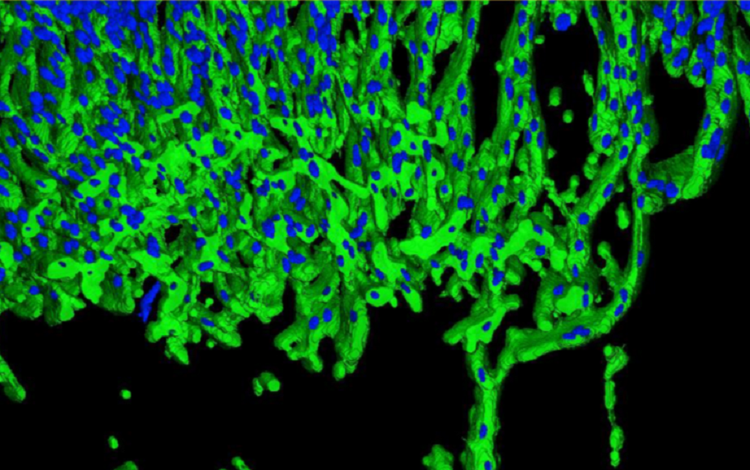
3D-Analyse angiogener Sprossen (grün) und Zellkerne (blau) mit der MetaXpress® High-Content Image Acquisition and Analysis Software.
Neuritenauswuchs
Die Entwicklung von Wirkstoffen für neurodegenerative Erkrankungen erfordert ein gründliches Verständnis der Verbindungen zwischen Neuronen. Diese Verbindungen, vermittelt durch die erweiterten neuronalen Strukturen auf Zellen, die als Axone und Dendriten bezeichnet werden, werden als Neuriten definiert. Daher ist das Neuritenauswachsen ein signifikanter Indikator für neuronale Konnektivität oder Störungen darin.
Neuritenauswuchs-Assays können dabei helfen, intrazelluläre und extrazelluläre Signale, die an der neuronalen Degeneration beteiligt sind, zu visualisieren und quantitativ zu analysieren. Dies erfordert jedoch physiologisch relevante 3D-Gewebemodelle.
Um die Inhibition des Neuritenauswuchses zu untersuchen, nutzten Forscher von MIMETAS die OrganoPlate-Plattform, um auf Mikrofluidik basierende und nachhaltige neuronale Kulturen zu entwickeln. Wie im High-Content Assay for Morphological Characterization of 3D Neuronal Networks in a Microfluidic Platform gezeigt, wurden aus iPSC gewonnene humane Neuronen mit Verbindungen behandelt, die das Neuritenauswuchswachstum hemmten und mit drei verschiedenen Farbstoffen differenzialgefärbt wurden.
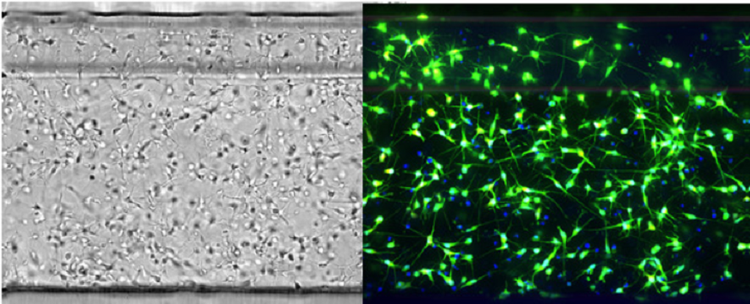
iCell-Neuronen in OrganoPlate-Kapillarzellen für 72 Stunden (links) und Lebendzellen, die mit drei Farbstoffen gefärbt wurden, untersucht mit dem ImageXpress® Micro Confocal High-Content Imaging System (rechts).
Das ImageXpress Micro Confocal High-Content Imaging System unterstützte die Beurteilung der neuronalen Überlebensfähigkeit sowie morphologischer Veränderungen in Neuronen. Die 3D-Analyse mit der MetaXpress Software lieferte quantitative Daten wie die Anzahl der Neuriten, das Neuronenvolumen, die Anzahl der Kerne und die Anzahl der Neuritenverzweigungen.
Die Ergebnisse belegen, dass die Kombination von MIMETAS’ OrganoPlate und Molecular Devices’ High-Content-Imaging-Systemen zur Beurteilung der Wirksamkeit und Toxizität neurologischer Wirkstoffe eingesetzt werden kann.
Erste Schritte mit 3D-Modellen für menschliches Gewebe und Imaging
Die effiziente Implementierung von Organ-on-a-Chip-Systemen erfordert ein gründliches Verständnis des Arbeitsmechanismus. Glücklicherweise sind alle Informationen, die Sie benötigen, nur einen Klick entfernt.
In, Erste Schritte mit 3D Human Tissue and Imaging , zeigen Chiwan Chiang (Field Application Scientist, MIMETAS) und Oksana Sirenko, PhD (Sr. Applications Scientist, Molecular Devices), wie Sie schnell, einfach und kostengünstig aussagekräftige neue Erkenntnisse aus diesen Modellen gewinnen können.
Tauchen Sie in die Einrichtung organotypischer 3D-Gewebemodelle in der OrganoPlate ein und entdecken Sie die Rolle des High-Content-Imaging in Organ-on-a-Chip-Studien. Die Referenten diskutieren die Vorteile der Modellierung menschlicher Gewebe mit zwei Fallstudien. Fallstudie Eins, Darm-on-a-Chip, umfasst das Caco-2-Darmmodell zur Beurteilung der Barriereintegrität. Die zweite Fallstudie, die Angiogenese, bezieht sich auf die Angiogenese in HUVEC-Mikrogefäßen.
Benötigen Sie Hilfe bei Ihrem Organ-on-a-Chip-Arbeitsablauf?
Erfahren Sie mehr über unser Organoid Innovation Center und unser umfangreiches Portfolio an Lösungen.
