
Organoide von kolorektalen Karzinomen (CRC)
Aus Patienten stammende kolorektale Krebsorganoide (CRC)
Aus Darmkrebs-Patienten stammende Organoide (PDOs) sind dreidimensionale (3D) Zellkulturmodelle, die die Physiologie des Darmepithels und die genetischen Eigenschaften von Darmkrebspatienten nachbilden. Diese CRC-PDOs modellieren Zell-Zell-Interaktionen und den Zustrom von Sauerstoff und Nährstoffen innerhalb der Mikroumgebung des Tumors. Bei der Kultivierung im Labor dienen diese Tumor-Organoide als multizelluläre Mini-Nachbildungen des 3D-Tumors, und sie haben die Fähigkeit bewiesen, ihre In-vivo-Eigenschaften beizubehalten.
CRC-Organoide (und solche aus anderen Organen des Körpers) werden aus adulten Stammzellen gewonnen, die aus Patientenbiopsien isoliert wurden. Das Gewebe wird im Labor aufbereitet und in eine gelatinöse Basalmembran-Matrix eingebettet, die physischen Halt und Wachstumsfaktoren bietet. Die Stammzellen aus dem Gewebe teilen sich und bilden mehrere Zelltypen (einschließlich weiterer Stammzellen), die sich selbst zu dreidimensionalen Strukturen zusammenfügen und dabei die architektonische Konformation und Physiologie des ursprünglichen Tumors imitieren. Nach der Bildung dieser Strukturen können diese aufgespalten werden, um mehrere neue PDOs wieder auszusäen, die sich auf die gleiche Weise selbst zusammenfügen. Auf diese Weise lässt sich die Zahl der Organoide je nach Bedarf um eine Vielzahl weiterer Organoide erweitern.
Vorteile der aus Patienten stammenden kolorektalen Krebsorganoide
Durch die Darstellung der CRC-assoziierten genetischen Veränderungen und der Tumorzusammensetzung sind CRC-PDOs ideal für die Krebsforschung und die Wirkstoffforschung. Biologisch relevante CRC-PDOs können auf Wirkstoffe ähnlich reagieren wie Patienten, was auf ihren Wert bei der Prognose der Wirksamkeit neuer Therapeutika hinweist. Herkömmliche manuelle Arbeitsabläufe für Organoid-Assays eignen sich jedoch nicht für ein reproduzierbares Hochdurchsatz-Screening von Verbindungen in der Wirkstoffforschung.
Fortschritte bei der Skalierung von Organoiden und der Automatisierung von Assays haben dazu beigetragen, die Arbeitsabläufe für CRC PDOs zu standardisieren. Unsere 3D Ready Organoide werden in einer industriellen Umgebung unter Verwendung unserer firmeneigenen Bioreaktortechnologie und streng kontrollierter Prozesse hergestellt. Nun können in einer einzigen Charge viele Millionen standardisierte, gleichmäßig große und qualitätsgeprüfte Organoide erzeugt werden. Die CRC-Organoide werden kryokonserviert und können bei Bedarf für Assays mit hohem Durchsatz verwendet werden. Die Verwendung von Liquid Handlern, um die PDOs in Multiwell-Schalen zu plattieren und mit Verbindungen zu behandeln, reduziert Fehler und Zeitaufwand erheblich. Veränderungen nach der Behandlung mit Wirkstoffen können mit geeigneten Assays und Bildanalysen bewertet werden.
Arbeitsablauf bei der Kultivierung und Untersuchung von Darmkrebs-Tumoroiden
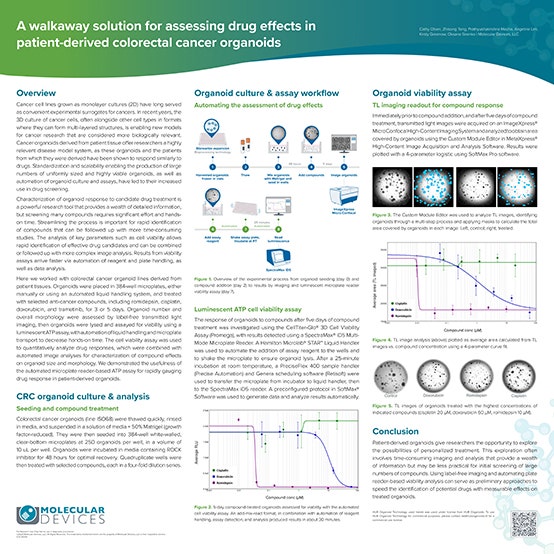
Die Bewertung der Wirkung von Wirkstoffen auf kolorektale Tumoroide kann automatisiert werden. Der nachstehende Arbeitsablauf zeigt die automatisierte Bewertung der Wirkung von Anti-Krebs-Verbindungen. Das Scale-up von PDOs erfolgt durch Erweiterung in einem Bioprozess mit Hilfe von Bioreaktortechnologie. Nach der Behandlung der Organoide mit dem zu prüfenden Wirkstoff wird die morphologische Analyse mit dem ImageXpress® Micro Confocal High-Content Imaging System durchgeführt, während der SpectraMax® iD5 Multimodus-Mikroplatten-Reader für die Prüfung der Überlebensfähigkeit verwendet wird. Der Arbeitsablauf umfasst eine automatisierte Inkubation und Flüssigkeitshandhabung sowie eine Planungssoftware für den Transfer der Platten vom Inkubator zum Liquid Handler und zum Platten-Reader.

Versuchsprotokoll für CRC-PDOs
- Organoid-Bioprozess – CRC-PDOs werden manuell erweitert und in Bioreaktoren ausgesät. Die entstehenden Organoide werden gezählt und bewertet, um ihren endgültigen Größenbereich zu bestimmen. Eine bestimmte Anzahl von Organoiden wird in Fläschchen gefüllt und kryokonserviert, so dass sie jederzeit Assay-fähig für den Benutzer zur Verfügung stehen.
- Auftauen – PDOs werden bei 37°C aufgetaut, mit frischem Medium gewaschen und pelletiert.
- Aussaat – PDOs werden in der erforderlichen Hydrogel- oder Basalmembran-Matrix suspendiert, um Multi-Well-Platten in der gewünschten Dichte auszusäen.
- Behandlung – 48 Stunden nach dem Aussäen können die PDOs in den Wells mit den zu prüfenden Verbindungen oder Wirkstoffen in den erforderlichen Konzentrationen behandelt werden.
- Imaging und Analyse – Das Durchlicht-Imaging (Transmitted Light, TL) wird fünf Tage nach der Behandlung mit der Verbindung durchgeführt, um die gewünschten Parameter wie die Anzahl der Organoide, den durchschnittlichen Durchmesser, das durchschnittliche Volumen, die von Organoiden bedeckte Gesamtfläche, die Morphologie usw. zu bestimmen.
- Überlebensfähigkeits-Assay – Ein Beispiel für ein Endpunkt-Assay-Protokoll
- Überlebensfähigkeits-Assay-Reagenz – Ein automatisierter Liquid Handler wird verwendet, um das Assay-Reagenz in die Wells für einen ATP-Lumineszenz-Assay zur Überlebensfähigkeit von Zellen zu geben, während das automatisierte Schütteln der Mikroplatte die Lyse der Zellen bewirkt.
- Inkubation – Die Inkubation erfolgt bei Raumtemperatur für 25 Minuten.
- ATP-Lumineszenz-Assay zur Überlebensfähigkeit von Zellen – Für den Transfer der Mikroplatte vom Inkubator zum Liquid Handler und zum Mikroplatten-Reader werden eine Planungssoftware und ein Proben-Handler eingesetzt. Die Ergebnisse werden mit einer Software zur Steuerung des Mikroplatten-Readers und zur Datenanalyse ausgewertet.
Wir bieten umfangreiche Laborautomatisierungslösungen für benutzerdefinierte Arbeitsabläufe bezüglich kolorektaler Organoide. Jeder Schritt – von der Organoidkultur und der Aussaat bis hin zur Flüssigkeitshandhabung und Bilderfassung – kann automatisiert und mit unseren Softwarelösungen für die Datenanalyse kombiniert werden, um regelkonforme und publikationsreife Berichte über Ihre Organoid-Assays zu erstellen.
Ausgewählte Assays
Eine Walkaway-Lösung zur Bewertung der Medikamentenwirkungen in aus Patienten stammenden kolorektalen Krebsorganoiden
In diesem wissenschaftlichen Poster wird berichtet, wie aus Patienten gewonnene kolorektale Organoide gezüchtet und mit den krebshemmenden Verbindungen Romidepsin, Cisplatin, Doxorubicin und Trametinib behandelt wurden.
Das labelfreie Durchlicht-Imaging zeigte als Reaktion auf die Wirkstoffbehandlung dosisabhängige Veränderungen der Organoidzahl und der Gesamtfläche, die von den Organoiden bedeckt wurde. Ein Plattenreader-basierter ATP-Lumineszenz-Assay ermöglichte es, quantitative Daten zur Überlebensfähigkeit von Zellen aus den Organoiden zu gewinnen.
Der Arbeitsablauf umfasst die automatisierte Handhabung von Flüssigkeiten, den Transfer von Mikroplatten und Software-Analysemethoden, um den Zeitaufwand zu verringern und das Wirkstoffscreening zu beschleunigen.
Neueste Ressourcen
Die Komplexität der kolorektalen Organoidstrukturen erfordert fortschrittliche Imaging- und Analysestrategien. Darüber hinaus müssen zeitaufwändige und arbeitsintensive Schritte automatisiert werden, um die Bearbeitungszeit zu verkürzen und die Konsistenz zu erhöhen. Erfahren Sie, wie eine qualitative und quantitative Analyse von Tumoroiden mit hohem Durchsatz durch Automatisierungsstrategien erreicht werden kann.