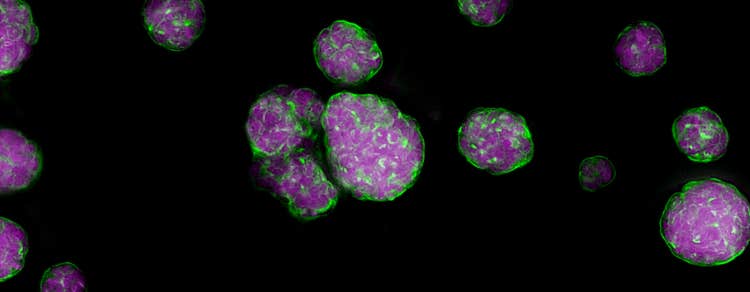
Sphäroide
Verwendung von Sphäroiden in der Krebsforschung und dem Wirkstoffscreening
Was sind Sphäroide?
Sphäroide sind dreidimensionale (3D) Zellaggregate, die Gewebe und Mikrotumore imitieren können. In den letzten Jahren wurden wesentliche Fortschritte bei der Entwicklung von In-vitro-Aggregaten aus Tumorzellen gemacht, die als Modelle für In-vivo-Gewebeumgebungen dienen. Wenn diese Aggregate in ein Well einer Platte mit Rundboden und äußerst geringer Bindung ausgesät werden, bilden sie jeweils ein separates Sphäroid.
Von Sphäroiden wird angenommen, dass sie das Verhalten von Tumoren wirksamer nachahmen als reguläre zweidimensionale (2D)-Kulturen. Der Grund ist, dass sie, wie Tumore, sowohl an der Oberfläche exponierte als auch tief verborgene Zellen, proliferierende und nicht-proliferierende Zellen, ein sauerstoffarmes Zentrum und eine gut mit Sauerstoff angereicherte äußere Zellschicht enthalten. Solche 3D-Sphäroid-Modelle werden in Screening-Umgebungen erfolgreich eingesetzt, um die Sicherheit von Wirkstoffen besser beurteilen zu können und um potentielle Krebstherapeutika zu identifizieren.
Die Verwendung von Sphäroiden in der Krebsforschung und dem Wirkstoffscreening
Eines der wichtigsten Ziele der Krebsforschung ist es, die Bildung von Tumorzellen zu verstehen. Im Vergleich zu 2D-Zellkulturen ahmen Sphäroide solide Tumore viel genauer nach. Sie helfen dabei, die physiologischen Veränderungen aufzuzeigen, die Tumorzellen von gesunden Zellen unterscheiden. Multizelluläre Tumor-Sphäroid-Modelle gewähren tiefere Einblicke in die Mikroumgebung des Tumors und ermöglichen es Forschern, Zell-Zell-Interaktionen, die Nährstoffaufnahme und die Proliferation von Tumorzellen zu visualisieren.
Sphäroide eignen sich zudem ideal für präklinisches Wirkstoffscreening und Validierung durch die Überwachung der zellulären Reaktionen auf therapeutische Interventionen. Insbesondere können sie die Fähigkeit (oder Unfähigkeit) von Wirkstoffen zur Tumorinfiltration sowie deren hemmende Wirkung auf die Metastasierung aufzeigen.
Die Stammzellforschung stellt ein weiteres wichtiges Anwendungsfeld von Sphäroiden dar, insbesondere mittels Kultivierung embryonaler (ESZ) und neuraler Stammzellen (NSZ). Kürzlich haben Forscher mesenchymale Stammzellen (MSZ) in Form von Sphäroiden kultiviert und deren regenerative und entzündungshemmende Wirkungen nachgewiesen, was ihr Potenzial für die regenerative Medizin und zellbasierte Therapien aufzeigt.
Im Vergleich zu anderen 3D-Zellkulturmethoden bieten Sphäroide mehrere Vorteile, einschließlich ihrer Relevanz für die Tumorbiologie, geringere Kosten, weniger Arbeitsaufwand als Tiermodelle, Reproduzierbarkeit sowie einfache Integration in das Hochdurchsatz-Screening und fortschrittliche Imaging-Techniken.
Arbeitsablauf zur Analyse von 3D-Sphäroiden mittels Hochdurchsatz-Screening
Das Imaging und die Analyse von Sphäroiden sind für das Verständnis der Entstehung und des Verhaltens von Tumormikroumgebungen entscheidend. Sie können auch dabei helfen, aus dem Screening für Krebsmedikamente aufschlussreichere und realistischere Daten zu erhalten. Hier haben wir Methoden zur Erzeugung von 3D-Sphäroiden sowie konfokale Imaging- und Analysemethoden für das Hochdurchsatz-Screening entwickelt und optimiert.
Sphäroide können in 96- oder 384-Well-Platten gezüchtet, mit Verbindungen behandelt und mit Farbstoffen gefärbt werden, die aktive zelluläre Prozesse und Signalwege sichtbar machen. In einigen Fällen können die Sphäroide ohne Waschen bildlich erfasst werden. Sie können auch fixiert werden, falls dies erwünscht ist.
Sphäroide kultivieren – Krebszellen können direkt in einer Platte mit äußerst geringer Bindung (ULA, ultra-low attachment), in Rundbodenplatten oder anderen Kulturplatten kultiviert werden, um die typische Morphologie eines Sphäroids zu entwickeln. Andere Kultivierungsplatten ermöglichen es, mehrere Sphäroide in einem einzigen Well wachsen zu lassen.
Mit Verbindungen behandeln – nachdem die Sphäroide ausgebildet sind, werden Verbindungen in den gewünschten Konzentrationen zu den Wells hinzugefügt und für einen Tag bis mehrere Tage inkubiert, je nachdem, welcher Mechanismus untersucht wird.
Auf Marker färben – nachdem die Behandlung mit Verbindungen abgeschlossen ist, werden die Farbstoffe direkt zum Medium hinzugegeben. Um eine Störung der Sphäroide zu vermeiden, können Färbungen angewendet werden, die keinen Waschschritt erfordern. Sphäroide können, wenn notwendig, jedoch auch vorsichtig gewaschen werden, sogar automatisiert.
Sphäroid-Abbildungen aufnehmen – mittels spezialisierter Imaging-Ausrüstung können Bilder vom Inneren des Sphäroid-Körpers einzeln oder als ein Z-Stapel (mehrere Bilder in verschiedenen Tiefen) aufgenommen werden.
Krebszellen analysieren – nutzen Sie eine Software für zelluläre Bildanalyse, um die Zellbilder quantitativ auszuwerten, um die Expression verschiedener Marker zu überwachen und um biologische Messungen zu quantifizieren.
Anwendung und Assays
Modernste 3D-Imaging- und Analysemethoden sind für die Charakterisierung, Reproduktion und Überwachung von Sphäroiden entscheidend. Ein so komplexer Arbeitsablauf kann von einer High-Content-Imaging- und Bildanalyse-Software stark profitieren. Erfahren Sie aus den unten aufgeführten Ressourcen mehr über unsere Methoden für die Sphäroid-Forschung.
Ressourcen zu Sphäroiden
Erkunden Sie unser High-Content-Imaging-Portfolio
High-Content-Imaging- und Analyse-Lösungen, angefangen bei automatisierter Digitalmikroskopie bis hin zu konfokalen High-Throughput-Imaging-Systemen mit Multi-Laser-Lichtquellen, Wasserimmersionsobjektiven und firmeneigener Spinning-Disk-Technologie sowie fortschrittlicher KI-Software.