3D-Organoide und Automatisierung komplexer Zell-Assays [Podcast]
Während wir mit Gentherapie und personalisierter Medizin in das Zeitalter der fortschrittlichen Wirkstoffforschung eintreten, müssen wir darauf vorbereitet sein, komplexe Erkrankungen zu untersuchen, die therapeutische Wirkung von Wirkstoffen zu beurteilen und unerwünschte Wirkungen zu identifizieren, die ein Risiko für die Gesundheit der Patienten darstellen können. Leider sind die aktuellen präklinischen Methoden, wie z. B. Tiermodelle oder 2D-Zellkulturen, unzureichend. Da die physikalischen und chemischen Eigenschaften dieser Modelle nicht den menschlichen Zustand repräsentieren, bedeutet die präklinische Arzneimittelbewertung keinen klinischen Erfolg. Aus diesem Grund kann die Entwicklung von 3D-Zellmodellen wie Organoiden ein großer Meilenstein für die Verbesserung der Wirksamkeit und Sicherheit von Wirkstoffen sein.
Dr. Oksana Sirenko ist Senior Manager of Assay Development bei Molecular Devices und arbeitet an der Entwicklung komplexer zellbasierter Modelle für die 3D-Biologie sowie High-Content-Imaging und Assay-Automatisierung.

In diesem Podcast-Auszug erörtert Senior Scientist Oksana die Vorteile von 3D-Zellmodellen und bewältigt gleichzeitig Herausforderungen im 3D-Zell-Imaging, wie Bildqualität, hoher Durchsatz, Automatisierung und Analyse.
Inhalt
1. Warum sind 3D-Zellmodelle und 3D-Organoide in der Krankheitsforschung und im Wirkstoffscreening so nützlich?
Das Hauptproblem in der aktuellen Krankheitsforschung und Wirkstoffentwicklung ist, dass nur etwa 3% der entwickelten Wirkstoffe in die Klinik gelangen. Die Mehrheit der Wirkstoffe scheitert in klinischen Studien aufgrund mangelnder Wirksamkeit oder unerwünschter Toxizitätsprobleme. Bessere Assaysysteme und Krankheitsmodelle sind erforderlich, um die Wirkstoffforschung zu erleichtern und den Erfolg in der Klinik besser vorherzusagen.
Heutzutage verlagert sich die Biologie in Richtung einer erhöhten Komplexität für Assays und Modelle, die für die Wirkstoffforschung und -entwicklung verwendet werden können. Es wird angenommen, dass 3D-Modelle die Lücke zwischen traditionellen zellbasierten Modellen und Geweben und Organen schließen. 3D-Modelle, die Sphäroide, Organoide und Organ-on-a-Chip umfassen, präsentieren eine Vielzahl von humanen Zelltypen, wie Leber, Immunzellen, Herzzellen und Fibroblasten. Zudem können sie die Morphologie menschlicher Gewebetypen nachahmen, wie z. B. das Wachstum von 3D-Tumoren, Krypten in Darmorganoiden, Nervenrohren oder den Fluss von Flüssigkeiten. Schließlich stellen sie zumindest einige Aspekte der Gewebefunktionalität dar, von der metabolischen Aktivität der Leber über den Schlag von Herzorganoiden bis hin zu Spitzen neuronaler Aktivität in Gehirnorganoiden. Diese größere Komplexität und Komplexität ermöglicht es uns, Prozesse im Gewebe, Interaktionen zwischen Zelltypen, Reaktionen auf Arzneimittel, Toxizitätseffekte und Prozesse der Wirkstoffpenetration in das Gewebe nachzuahmen.
https://share.vidyard.com/watch/savfn77oaeR6fQfcfJwZ54
Zerebrale Organoide zeigen eine Organisation, die an ein sich entwickelndes Gehirn erinnert.
2. Warum stellt die Komplexität von 3D-Modellen eine Hürde/Herausforderung für Forscher dar?
Herkömmliche 2D-Zell-Assays sind einfacher zu handhaben, aber 3D-Assays sind besser vorhersehbar und ermöglichen die Erzeugung von biologisch relevanteren Daten. Trotz des zunehmenden Interesses an der 3D-Forschung ist die breite Akzeptanz von Assays jedoch durch technische Hürden und die Komplexität von Assays begrenzt, was zu höheren Kosten, geringerem Durchsatz und mangelnder Reproduzierbarkeit führt. Eine größere Komplexität stellt Herausforderungen dar, aber Möglichkeiten für die Geräteentwicklung und Automatisierungsentwicklung würden es Wissenschaftlern ermöglichen, 3D-Assays mit größerem Durchsatz und höherer Genauigkeit durchzuführen.
3. Können Sie einen typischen Arbeitsablauf für die Entwicklung und Analyse von 3D-Organoiden beschreiben?
Der typische Arbeitsablauf für Organoid-Assays umfasst eine Reihe von Schritten, und dieser Prozess ist üblicherweise viel länger als 2D-Arbeitsablaufschritte.
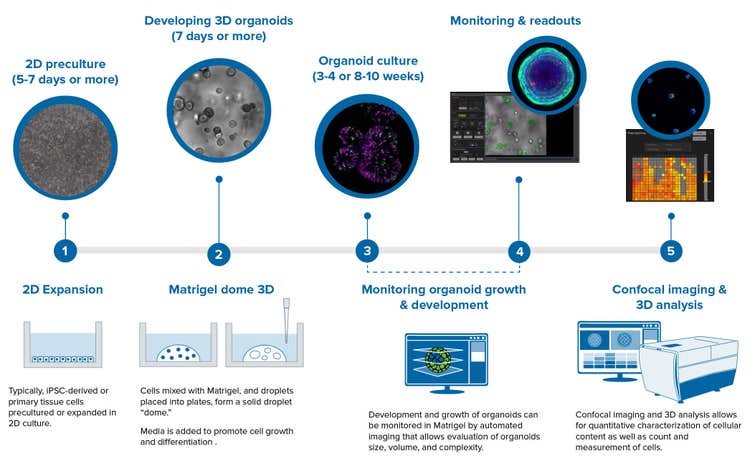
3D-Organoide können aus primären Zellen wie Darmorganoiden oder induzierten pluripotenten Stammzellen (iPSCs), z. B. neuronalen oder kardialen Organoiden, gewonnen werden. Der Arbeitsablauf kann von der 2D-Vorkultur oder der Expansion von iPSC-Zellen beginnen, gefolgt vom Differenzierungsschritt. Danach werden die Zellen mit Matrigel vermischt und typischerweise innerhalb der Matrigel-Dome entwickelt, was auch das Passieren und die Expansion umfassen kann. Darmorganoide, kolorektale, pankreatische und Leberorganoide werden üblicherweise mit diesem Matrigel-Dome-Schritt entwickelt.
Alternativ benötigen einige andere Organoidtypen kein Matrigel, sondern werden in Platten mit geringer Bindung (z. B. Herzorganoide) entwickelt.
Die Entwicklung von Organoiden dauert einige Tage bis zu mehreren Wochen. Einige Protokolle benötigen sogar ein paar Monate. Dies ist ein sehr langwieriger Prozess und wird von der Automatisierung erheblich profitieren.
Schließlich wird der Endpunkt-Assay, ob es sich um eine Arzneimittelbehandlung, einen Virusinfektiositäts-Assay oder eine Toxizitätsbewertung handelt, in einem Multi-Well-Format mit 96 oder 384-Well-Platten eingerichtet.
Anschließend werden die Zellen mit Wirkstoffen behandelt und für Messungen verarbeitet, die ATP-Assays, Zelltod-Assays, High-Content-Imaging oder Calciumoszillation umfassen können.
4. Können Sie mir etwas darüber erzählen, wie Sie Arbeitsabläufe für 3D-Zellmodelle speziell auf Ihre Forschung anwenden?
Wir konzentrieren uns auf die Entwicklung von Automatisierungsprotokollen für automatisierte Zellkulturen sowie auf das automatisierte Imaging und die Bildanalyse für komplexe 3D-Arbeitsabläufe. Kürzlich haben wir automatisierte Screening-Assays entwickelt und durchgeführt, um effizientere Krebsmedikamente für dreifach-negativen Brustkrebs zu finden. Wir verwendeten von Patienten stammende Krebsorganoide, die einen arzneimittelresistenten Krankheitsphänotyp repräsentieren, und verwendeten Automatisierung für Kultur-3D-Organoide, simulierte Wirkstoffinterventionen und führte Endpunkt-Assays zur Identifizierung der Verbindungen durch, die Tumorzellen abtöten. Wir testeten eine Bibliothek von Verbindungen und fanden mehrere Kandidaten, die eine höhere Wirksamkeit aufwiesen als aktuelle Standardmedikamente.
5. Können Sie erklären, wie der Arbeitsablauf für die Entwicklung und Analyse von Organoiden automatisiert wird?
Wir haben bei Molecular Devices eine automatisierte Arbeitszelle entwickelt, die mehrere Instrumente in einem komplexen System kombiniert. Es umfasst einen automatisierten Pipettierroboter von Beckman Biomek, einen automatisierten LiCONiC-Inkubator, unser ImageXpress HT.ai High-Content-Imaging-System, unseren SpectraMax Plattenreader und AquaMax-Waschersowie eine automatisierte Bionex-Zentrifuge. Alle Komponenten sind über einen kollaborativen Roboter, PreciseFlex, verbunden400, der die Platten zu den gewünschten Zeitpunkten von einem Gerät zum anderen bewegen kann, während die Planungssoftware sicherstellt, dass alle Systemelemente nahtlos zusammenarbeiten. Jedes Gerät verfügt über mehrere Protokolle, die für verschiedene Schritte entwickelt wurden, einschließlich der Fütterung der Zellen und der Organoid-Plattierung, die vom Planer zu bestimmten Zeiten aufgerufen werden können.

Das neue Organoid Innovation Center von Molecular Devices kombiniert modernste Technologien mit neuartigen Methoden der 3D-Biologie, um die wichtigsten Herausforderungen der Skalierung der komplexen 3D-Biologie zu lösen.
Imaging-Methoden sind ein weiterer spannender Bereich der Technologie für die Organoidforschung. Um Organoide oder Organ-on-a-Chip abzubilden, müssen wir eine fortschrittliche Optik verwenden. Das ImageXpress High-Content-Imaging-System bietet mehrere Vorteile für 3D-Proben:
Leistungsstarke Laser und konfokale Optik ermöglichen es uns, den Z-Stapel mehrerer Bilder von unten nach oben aufzunehmen, mit Schritten wie 5–10 μm. Die konfokale Optik ermöglicht es uns, das Licht, das außerhalb des Fokus liegt, abzuweisen, sodass wir schärfere Bilder über Organoide und Matrigel hinweg erhalten können.
Als Nächstes analysiert unsere MetaXpress Bildanalysesoftware die Bilder in jedem 2D-Schnitt und wandelt Daten in 3D-Raum um. Sie können mehrere Messungen durchführen, um Organoide, Zellen oder subzelluläre Organellen zu charakterisieren. Diese Messungen helfen bei der Definition von Zellzahlen, -intensitäten, -volumina, -flächen, -abständen und mehr und ermöglichen es uns, Veränderungen der Morphologie, des Zellgehalts und der Überlebensfähigkeit zu überwachen und zu quantifizieren. Darüber hinaus verfügen wir über Elemente des maschinellen Lernens, bei denen Anwender Software trainieren können, um Objekte und Funktionen zu erkennen und so eine effizientere und aufschlussreichere Analyse zu ermöglichen.
6. Wie kann Automatisierung speziell bei der Erforschung komplexer Systeme helfen?
Die Automatisierung würde den Arbeitsaufwand und wiederholte Aufgaben wie das Füttern von Zellen jeden Tag oder jeden zweiten Tag über 2 Monate hinweg reduzieren. Außerdem wird es helfen, die Forschung mit höherem Durchsatz zu beschleunigen. Anstatt zum Beispiel 3 Zelllinien oder 5Mutationen zu untersuchen, würde die Automatisierung es Ihnen ermöglichen, 50 Zelllinien auf 100Mutationen zu testen.
High-Content-Imaging mit Hilfe von maschinellen Lernalgorithmen ermöglicht es, eine Vielzahl von Veränderungen in Organoiden und Zellen zu beobachten und zu charakterisieren. Dies ermöglicht mehrere Messungen und liefert wertvolle Informationen über Zellwachstum, Differenzierung, Zellzyklus, Tod, Apoptose, Genexpression oder Aktivierung von Signalwegen.
7. Wie werden Sie diese Systeme in Ihrer zukünftigen Forschung wieder einsetzen?
Zusätzlich zu den Studien zur Krebsbiologie entwickeln wir aktiv weitere Arbeitsabläufe, einschließlich, aber nicht beschränkt auf Darmorganoide, Stammzell-Arbeitsablauf, Herzorganoide und mehr.
8. Wie wird sich die Automatisierung der 3D-Organoidanalyse in Zukunft weiterentwickeln?
Wir glauben, dass die Automatisierung mit der Entwicklung der Biologie und der zunehmenden Komplexität von Assays immer wichtiger werden wird, um Krankheitsmechanismen besser zu verstehen, die Wirkstoffforschung zu beschleunigen und schließlich bessere Wege zur Behandlung von Krankheiten zu finden.
Durch die Entwicklung neuer und fortschrittlicherer Technologien und Instrumente sind wir davon überzeugt, dass wir weiter zum Fortschritt der Life Science beitragen werden.
Das Verständnis der Grundprinzipien hinter 3D-Organoiden – und der aktuellen Engpässe – ist für die erfolgreiche Entwicklung und Nutzung dieser fortschrittlichen Modelle für die Wirkstoffforschung von entscheidender Bedeutung.
Hören Sie sich den vollständigen Podcast an
Wenn Sie mehr erfahren möchten, genießen Sie bitte den vollständigen Podcast „Komplexe Assays mit Ian Shoemaker, Beckman Coulter Life Sciences und Dr. Oksana Sirenko, Molecular Device“.
Prüfung des Wirkstoffziels · Episode 14 – Ian Shoemaker, Beckman Coulter und Dr. Oksana Sirenko, Molecular Devices
Hier diskutieren sie einen umfassenden Überblick über die Wissenschaft der Organoidforschung – entdecken Sie, wie Organoidmodelle entwickelt und in der Forschung unserer Experten verwendet werden und wie sich die Automatisierung der 3D-Organoidanalyse in Zukunft weiterentwickeln wird, und vieles mehr!